医療機器市場への参入
高齢化の更なる進展と新興国における医療の需要拡大に伴い、世界および日本の医療機器市場は今後さらに拡大することが見込まれています。
サン・フレアでは、医療機器体制の構築から製品上市までの各ポイントに応じたコンサルティングを提供し、医療機器ビジネスの事業化を支援いたします。
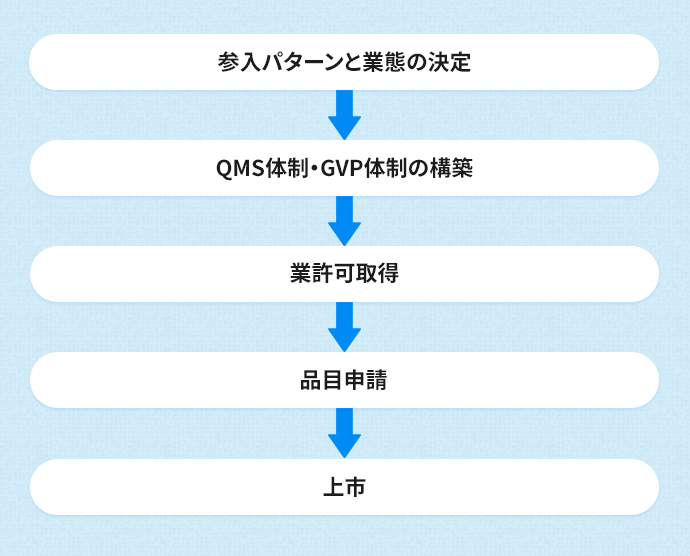
医療機器市場参入の流れ
高齢化の更なる進展と新興国における医療の需要拡大に伴い、世界および日本の医療機器市場は今後さらに拡大することが見込まれています。
サン・フレアでは、医療機器体制の構築から製品上市までの各ポイントに応じたコンサルティングを提供し、医療機器ビジネスの事業化を支援いたします。

医療機器市場参入プロジェクト
(過去11年間)
医療機器事業への参入パターンと業態取得に関するレクチャーを実施いたします。
QMS省令・ISO 13485に基づいた品質マネジメントシステム(QMS)およびGVP省令に基づいた市販後安全管理体制(GVP)の構築・運用・維持支援を行います。
製造販売業、製造業、販売・貸与業、修理業の取得支援に関するコンサルティングを行います。
「日本国内における薬事支援」のページをご覧ください。
下記フォームよりお問い合わせください。